
Metabolizma Yaşamı Şekillendiriyor: Glikoliz Erken Embriyonik Hücre Kararlarını Nasıl Yönlendiriyor
Max Planck Moleküler Hücre Biyolojisi ve Genetik Enstitüsü ile EMBL Barselona’nın yeni araştırmaları, glikolizin embriyonik gelişimde enerji sağlamanın ötesinde, hücrelerin doku türlerini belirlemede kritik bir rol oynadığını gösteriyor. Fare embriyonik kök hücreleriyle yapılan çalışmalar, glikolizin sinyal yollarını aktive ederek mezoderm ve endoderm oluşumunu desteklediğini ortaya koydu. Bu bulgular, metabolizmanın erken gelişimdeki önemini vurguluyor ve doku biyolojisi için yeni bir paradigmayı başlatıyor.
Glikolizin Embriyonik Gelişimdeki Rolü
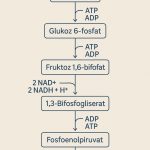
Glikoliz, şekeri enerjiye dönüştüren eski bir metabolik süreçtir ve hücrelerin büyümesi, bölünmesi ve hayatta kalması için temel bir rol oynar. Tek hücreli organizmalardan karmaşık memelilere kadar yaşamın başlangıcından beri var olan bu süreç, enerji sağlamanın ötesinde, erken embriyonik gelişimde hücrelerin kader kararlarını yönlendiren bir düzenleyici olarak ortaya çıkıyor.
Max Planck Moleküler Hücre Biyolojisi ve Genetik Enstitüsü (MPI-CBG) ve EMBL Barselona’dan araştırmacılar, glikolizin sadece enerji kaynağı olmadığını, aynı zamanda embriyonik kök hücre modellerinde hücrelerin belirli doku türlerine yönelmesini kontrol ettiğini gösteriyor. Cell Stem Cell dergisinde art arda yayınlanan iki çalışma, fare embriyonik kök hücrelerinden oluşan gastruloid ve gövde benzeri yapılar kullanarak vücut planının oluşumunun erken adımlarını inceledi.
Çalışmalar Nasıl Yapıldı?
Birinci Çalışma: Glikolizin Sinyal Rolü
EMBL Barselona’dan Dr. Vikas Trivedi liderliğindeki ekipte çalışan ve 2025’ten itibaren Viyana’daki Moleküler Biyoteknoloji Enstitüsü’nde (IMBA) grup lideri olacak Dr. Kristina Stapornwongkul, glikolizin rolünü anlamak için hücrelerin yaşadığı ve beslendiği ortamdaki glikoz konsantrasyonunu değiştirdi.
Glikoliz engellendiğinde, iki önemli doku türünün oluşumu bozuldu:
- Mezoderm: Kaslar, kemikler ve kan gibi yapılara dönüşür.
- Endoderm: Karaciğer ve akciğer gibi organları oluşturur.
Bunun yerine, hücreler ektoderm (sinir sistemine dönüşen doku) olmaya yöneldi. Araştırmacılar, glikolizin Wnt, Nodal ve Fgf gibi temel sinyal yollarını aktive ederek mezoderm ve endoderm kaderlerini desteklediğini buldu. Glikoliz engellendiğinde bu sinyaller zayıfladı, ancak sinyaller yapay olarak güçlendirildiğinde, glikoliz olmadan bile normal hücre kaderi kararları restore edildi.
Dr. Stapornwongkul, “Glikolizin çift rolü beni çok şaşırttı: büyüme için biyoenerjetik işlevi ve hücre kaderi kararları için sinyal işlevi. Glikolizi inhibe ettiğimizde, endoderm ve mezoderm kaybını net bir şekilde gördük, ancak sinyal yollarını aktive ederek bu hücre türlerini glikoliz olmadan bile kurtarabildik,” diyor.
Dr. Trivedi, “Metabolizma ve sinyalizasyon arasındaki hiyerarşik ilişki, organizma gelişiminin en erken aşamalarında heyecan verici. Bu, metabolizmanın çok hücreliliğin kökenindeki rolü hakkında merak uyandırıyor,” diye ekliyor.
İkinci Çalışma: Metabolik Denge ve Model Varyasyonu
MPI-CBG’den Dr. Jesse Veenvliet liderliğindeki ekipte çalışan doktora öğrencileri Alba Villaronga-Luque ve Ryan Savill, gövde benzeri yapıların neden bazılarının doğal embriyoya daha çok benzediğini araştırdı. Bu yapılar, omurga (mezoderm) ve omurilik (ektoderm) gibi dokuları oluşturan embriyonik gövde gelişim modelleridir.
Ekip, makine öğrenimi kullanarak görüntüleme verilerini, aktif gen profillerini ve metabolitleri zaman içinde entegre etti. Bulgular, glikoliz ile oksidatif fosforilasyon (enerji üretiminin başka bir süreci) arasındaki dengenin, bu yapıların varyasyonunu etkilediğini gösterdi. Glikolize daha bağımlı olan (şekeri parçalayarak enerji üreten) yapılar, embriyoya en çok benzeyenlerdi. Daha az glikolize bağımlı olanlar ise çoğunlukla ektoderm oluşturdu.
Villaronga-Luque, “Bu varyasyonun nedenini anlamak için, gelişimin erken aşamalarında ölçümler yapmamız gerekiyordu, ancak bu ölçümler genellikle örneği yok eder. Makine öğrenimiyle bu zorluğu aştık,” diyor.
Savill, “Kantitatif görüntüleme analizi ve makine öğrenimiyle, yapıların gelişim sonucunu öngören temel özellikleri bulduk. Bu öngörü gücüyle, son durumu bilinmeyen yapıların ifade profillerini araştırabildik,” diye ekliyor.
Ekip, glikolizi ilaçlarla artırarak gövde benzeri yapıların görünümünü iyileştirdiğini gösterdi. Dr. Veenvliet, “Erken metabolik durumun, modelin embriyoya ne kadar benzediğini kontrol ettiğini gösterdik. Bu öngörü gücü, hastalık modellemesi ve toksisite çalışmaları gibi yüksek tekrarlanabilirlik gerektiren uygulamalarda büyük potansiyel taşıyor,” diyor.
Neden Önemli?
Bu çalışmalar, glikolizin embriyonik gelişimde enerji sağlamanın ötesinde bir rol oynadığını gösteriyor. Glikoliz, sinyal yollarını aktive ederek hücrelerin hangi doku türüne dönüşeceğini düzenliyor. Bu, metabolizmanın erken gelişimdeki önemini vurgulayan yeni bir paradigmayı başlatıyor.
Ayrıca, kök hücre tabanlı embriyo modellerindeki varyasyonu azaltmak için metabolik düzenlemelerin kullanılabileceğini gösteriyor. Bu, hastalık modellemesi, genetik taramalar ve toksisite çalışmaları gibi alanlarda daha güvenilir modeller geliştirilmesine olanak tanıyabilir.
Gelecek İçin Öneriler
Araştırmacılar, glikolizin farklı embriyogenez aşamalarındaki etkilerinin daha fazla incelenmesi gerektiğini belirtiyor. Ayrıca, metabolik manipülasyonların diğer organoid modellerine uygulanması, doku biyolojisi ve gelişim biyolojisi alanlarında yeni keşiflere yol açabilir.
Yayın Tarihi ve Kaynak
Yayın Tarihi: 16 Nisan 2025
Kaynak: Max Planck Moleküler Hücre Biyolojisi ve Genetik Enstitüsü (MPI-CBG)
Referanslar:
- Alba Villaronga-Luque, Ryan G. Savill, Natalia López-Anguita, Adriano Bolondi, Sumit Garai, Seher Ipek Gassaloglu, Roua Rouatbi, Kathrin Schmeisser, Aayush Poddar, Lisa Bauer, Tiago Alves, Sofia Traikov, Jonathan Rodenfels, Triantafyllos Chavakis, Aydan Bulut-Karslioglu, Jesse V. Veenvliet. Integrated Molecular-Phenotypic Profiling Reveals Metabolic Control of Morphological Variation in a Stem-Cell-Based Embryo Model. Cell Stem Cell, 2025; DOI: 10.1016/j.stem.2025.03.012
- Kristina S. Stapornwongkul, Elisa Hahn, Patryk Poliński, Laura Salamó Palau, Krisztina Arató, LiAng Yao, Kate Williamson, Nicola Gritti, Kerim Anlas, Mireia Osuna Lopez, Kiran R. Patil, Idse Heemskerk, Miki Ebisuya, Vikas Trivedi. Glycolytic Activity Instructs Germ Layer Proportions through Regulation of Nodal and Wnt Signaling. Cell Stem Cell, 2025; DOI: 10.1016/j.stem.2025.03.011












İlk yorum yapan siz olun